Hongos nematófagos en el biocontrol de Meloidogyne exigua Goeldi en Coffea arabica L. var. Catimor, en Satipo – Perú
DOI:
https://doi.org/10.51252/raa.v2i2.343Palabras clave:
control, dosis, Paecilomyces, Pochonia, TrichodermaResumen
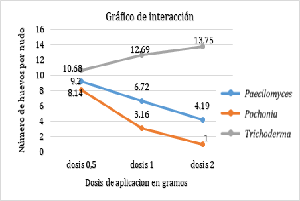
La selva central del Perú es la región más importante de producción de café a nivel nacional, donde observa una alta incidencia de nemátodo formador de agallas en las raíces del cafeto; Meloidogyne exigua Goeldi, no tiene un control adecuado ya que el control químico afecta la salud y el medio ambiente, en ese sentido se busca alternativas de control biológico. El objetivo fue probar la eficacia de tres hongos nematófagos contra M. exigua Goeldi utilizando plantas de vivero. El trabajo se realizó en laboratorio y campo. Las variables evaluadas fueron: número de agallas, incidencia de nematodo, severidad, población de huevos, población de juveniles 2 y población de hembras. Los resultados muestran que 1a aplicación de Pochonia chlamidosporia supera estadísticamente en el control de nematodos respecto a Paecilomyces lilacinus y Trichoderma harzianum, que ocupan el segundo y tercer lugar respectivamente. La dosis de 2 g/plántula para P. chlamidosporia supera estadísticamente a las dosis de 1,0 y 0,5 g/plántula. Cuando aumenta la dosis de aplicación de Paecilomyces lilacinus y Pochonia chlamydosporia disminuyen todas las variables; pero cuando aumenta la dosis de Trichoderma harzianum las variables permanecen constantes, por lo que no tiene efecto de control.
Descargas
Citas
Bontempo, A. F., Fernandes, R. H., Lopes, J., Freitas, L. G., & Lopes, E. A. (2014). Pochonia chlamydosporia controls Meloidogyne incognita on carrot. Australasian Plant Pathology, 43(4), 421–424. https://doi.org/10.1007/s13313-014-0283-x
Cleopas C., C., Kwasi S., Y., & Mark D., L. (2017). Biological control of the rootknot nematode, Meloidogyne javanica (Chitwood) using Bacillus isolates, on soybean. Biological Control, 109, 37–41. https://doi.org/10.1016/j.biocontrol.2017.03.009
Dube, B., & Grover C., S. J. (1987). Biological Control of Meloidogyne incognita by Paecilomyces lilacinus and Pasteuria penetrans. Journal of Nematology, 19(2), e227. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2618639/
Esteves, I., Peteira, B., Atkins, S. D., Magan, N., & Kerry, B. (2009). Production of extracellular enzymes by different isolates of Pochonia chlamydosporia. Mycological Research, 113(8), 867–876. https://doi.org/10.1016/J.MYCRES.2009.04.005
Flores-Camacho, R., Manzanilla-López, R. H., Cid del Prado-Vera, I., & Martínez-Garza, Á. (2007). Control de Nacobbus aberrans (Thorne) Thorne y Allen con Pochonia chlamydosporia (Goddard) Gams y Zare. Revista Mexicana de Fitopatología, 25(1), 26–35. http://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S0185-33092007000100004
Hoedekie, A., Viaene, N., & Van Damme, V. (2005). Long-term efficacy of Pochonia chlamydosporia for management of Meloidogyne javanica in glasshouse crops. Nematology, 7(5), 727–736. https://doi.org/10.1163/156854105775142973
Larriba, E., Jaime, M. D. L. A., Carbonell-Caballero, J., Conesa, A., Dopazo, J., Nislow, C., Martín-Nieto, J., & Lopez-Llorca, L. V. (2014). Sequencing and functional analysis of the genome of a nematode egg-parasitic fungus, Pochonia chlamydosporia. Fungal Genetics and Biology, 65, 69–80. https://doi.org/10.1016/j.fgb.2014.02.002
Luambano, N. D., Manzanilla-López, R. H., Kimenju, J. W., Powers, S. J., Narla, R. D., Wanjohi, W. J., & Kerry, B. R. (2015). Effect of temperature, pH, carbon and nitrogen ratios on the parasitic activity of Pochonia chlamydosporia on Meloidogyne incognita. Biological Control, 80, 23–29. https://doi.org/10.1016/J.BIOCONTROL.2014.09.003
Manzanilla-López, R. H., Esteves, I., Finetti-Sialer, M. M., Hirsch, P. R., Ward, E., Devonshire, J., & Hidalgo-Díaz, L. (2013). Pochonia chlamydosporia: Advances and Challenges to Improve Its Performance as a Biological Control Agent of Sedentary Endo-parasitic Nematodes. Journal of Nematology, 45(1), 7. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3625126/
Mendoza, G. A. ., Wilson, J. H. ., & Colina, J. C. (2013). Efecto de Trichoderma atroviride, Trichoderma harzianum y Trichoderma viride sobre huevos de Meloidogyne sp. en condiciones de laboratorio. Revista Científica de Estudiantes Rebiolest, 1(2), e65. https://revistas.unitru.edu.pe/index.php/ECCBB/article/view/479
Morton, C. O., Hirsch, P. R., Peberdy, J. P., & Kerry, B. R. (2003). Cloning of and genetic variation in protease VCP1 from the nematophagous fungus Pochonia chlamydosporia. Mycological Research, 107(1), 38–46. https://doi.org/10.1017/S0953756202007050
Puertas, A., De la Noval Pons, B. M., Martinez, B., Miranda, I., Felix, F., & Hidalgo-Diaz, L. (2006). Interacción de Pochonia chlamydosporia var. catenulata con Rhizobium sp., Trichoderma harzianum y Glomus clarum en el control de Meloidogyne incognita. Revista de Protección Vegetal, 21(2), 80–89. https://agris.fao.org/agris-search/search.do?recordID=CU2009100416
Puertas, A., & Hidalgo Díaz, L. (2009). Efecto de diferentes abonos orgánicos sobre el establecimiento de Pochonia chlamydosporia var.catenulata en el sustrato y la rizosfera de plantas de tomate. Revista de Protección Vegetal, 24(3), 165. http://revistas.censa.edu.cu/index.php/RPV/article/view/457
Publicado
Cómo citar
Número
Sección
Licencia
Derechos de autor 2022 Jose M. Alomia-Lucero, Eliseo Capcha-Ospina

Esta obra está bajo una licencia internacional Creative Commons Atribución 4.0.
Los autores retienen sus derechos:
a. Los autores retienen sus derechos de marca y patente, y tambien sobre cualquier proceso o procedimiento descrito en el artículo.
b. Los autores retienen el derecho de compartir, copiar, distribuir, ejecutar y comunicar públicamente el articulo publicado en la Revista Agrotecnológica Amazónica (RAA) (por ejemplo, colocarlo en un repositorio institucional o publicarlo en un libro), con un reconocimiento de su publicación inicial en la RAA.
c. Los autores retienen el derecho a hacer una posterior publicación de su trabajo, de utilizar el artículo o cualquier parte de aquel (por ejemplo: una compilación de sus trabajos, notas para conferencias, tesis, o para un libro), siempre que indiquen la fuente de publicación (autores del trabajo, revista, volumen, número y fecha).





